Изменение давления при нагревании, второй закон Гей-Люссака
Если
| pt | давление газа при произвольной температуре t, | Па |
|---|---|---|
| p0 | давление газа при температуре 0°С, | Па |
| t | температура, | 0°С |
| β | термический коэффициент давления (коэффициент объемного расширения газа), | 1/K |
то
\[ p_t = p_0 ( 1 + βt ) \]
Из формулы (1) следует, что при температуре t1
\[ p_1 = p_0 ( 1 + βt_1 ) \]
\[ p_1 = p_0 \bigg( 1 + \frac{t_1}{273.15} \bigg) \]
\[ p_1 = p_0 \bigg( 1 + \frac{t_1}{T_0} \bigg) \]
\[ p_1 = p_0 \bigg( \frac{T_0 + t_1}{T_0} \bigg) \]
а при другой температуре t2 соответственно
\[ p_2 = p_0 ( 1 + β t_2 ) \]
\[ p_2 = p_0 \bigg( 1 + \frac{t_2}{273.15} \bigg) \]
\[ p_2 = p_0 \bigg( 1 + \frac{t_2}{T_0} \bigg) \]
\[ p_2 = p_0 \bigg( \frac{T_0 + t_2}{T_0} \bigg) \]
Разделив первое равенство на второе, получим
\[ \frac{p_1}{p_2} = \frac{T_0 + t_1}{T_0 + t_2} \]
или
\[ \frac{p_1}{p_2} = \frac{T_1}{T_2} \]
или
\[ \frac{p}{T} = \const \]
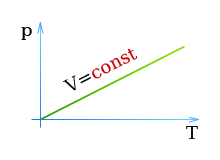
Второй закон Гей-Люссака
Второй закон Гей-Люссака гласит: Давление газа p в замкнутом объеме пропорционально абсолютной температуре газа T
\[ p \sim T \qquad (\enspace V = \const \enspace) \]
Формула (11) точно выполняется для идеальных газов, для реальных газов она является хорошим приближением и неприменима в случае пара.
Изменение давления при нагревании, второй закон Гей-Люссака |
стр. 525 |
|---|
